Bộ Y tế cho biết, quyết định này căn cứ theo đề xuất của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc đối với vắc xin, sinh phẩm và theo đề nghị của Viện Vệ sinh dịch tễ Trung ương.
Vắc xin Sinopharm còn có tên gọi là SARS-CoV-2 vaccine (Vero Cell) do Viện Sản phẩm sinh học Bắc Kinh thuộc Tập đoàn Biotec quốc gia Trung Quốc (CNBG) sản xuất. Mỗi liều 0,5ml chứa 6.5U kháng nguyên SARS-CoV-2 bất hoạt. Đây là vắc xin thứ 3 được cấp phép khẩn cấp tại Việt Nam sau AstraZeneca và Sputnik V.
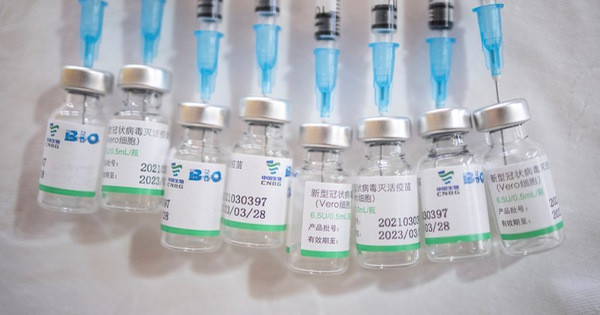
Vắc xin COVID-19 do Sinopharm phối hợp với Tập đoàn Công nghệ sinh học quốc gia Trung Quốc (CNBG)
Sau khi phê duyệt, Viện Vệ sinh Dịch tễ Trung ương có trách nhiệm phối hợp với nhà sản xuất phản hồi kịp thời các yêu cầu từ Bộ Y tế Việt Nam để bổ sung thêm dữ liệu hoặc các yêu cầu khác có liên quan đến vắc xin Sinopharm và chủ động cung cấp, cập nhật các thông tin mới liên quan đến vắc xin trong suốt quá trình phát triển sản phẩm.
Viện Vệ sinh Dịch tễ cũng được giao triển khai hệ thống cảnh giác dược toàn diện với vắc xin Sinopharm, phối hợp với Cục Khoa học công nghệ – Đào tạo và các đơn vị khác đánh giá tính toàn và hiệu quả của vắc xin Sinopharm.
Bộ Y tế giao Cục Quản lý dược cấp phép nhập khẩu vắc xin Sinopharm theo quy định; Cục Khoa học công nghệ và đào tạo lựa chọn đơn vị có đủ điều kiện đánh giá tính an toàn, hiệu quả của vắc xin trên cơ sở ý kiến tư vấn củ Hội đồng tư vấn sử dụng, vắc xin, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng; Cục Y tế dự phòng triển khai công tác tiêm chủng.
Vaccine Covid-19 của Sinopharm được Trung Quốc cấp phép vào ngày 24/12/2020, được Tổ chức Y tế Thế giới (WHO) phê duyệt khẩn cấp trong tháng 5/2021.
Hôm 27/5, hãng này công bố kết quả nghiên cứu thử nghiệm lâm sàng giai đoạn 3 trên Tạp chí Hiệp hội Y khoa Mỹ, cho biết vaccine có hiệu quả 78,1% trong ngăn ngừa các ca Covid-19 có triệu chứng và 73,5% các ca không triệu chứng.
Tính đến đầu tháng 5, khoảng 42 quốc gia và vùng lãnh thổ trên thế giới đang sử dụng vaccine Covid-19 của Sinopharm. Tổng số liều đã cung cấp là 200 triệu, sau vaccine của các hãng AstraZeneca, Pfizer-BioNTech và Moderna.
Ngoài ra, với các vaccine đã được các quốc gia khác phê duyệt nhưng chưa được WHO phê duyệt sử dụng trong tình trạng khẩn cấp, Bộ Y tế sẽ xem xét, phê duyệt trong thời gian 10 ngày làm việc khi nhận được đủ hồ sơ hợp pháp, hợp lệ và kèm theo ủy quyền chính thức của cơ sở sản xuất vaccine phòng Covid-19.
Khi làm thủ tục nhập khẩu vaccine vào Việt Nam, các đơn vị khẩn trương gửi hồ sơ chất lượng theo quy định (bao gồm: Giấy chứng nhận xuất xưởng của cơ sở sản xuất và/hoặc Giấy chứng nhận chất lượng của cơ quan quản lý) để Viện Kiểm định Quốc gia vaccine và sinh phẩm y tế (NICVB) thực hiện việc cấp Giấy chứng nhận xuất xưởng trong vòng 48 giờ theo khuyến cáo của WHO để đảm bảo chất lượng, tránh việc nhập khẩu vắc xin không rõ nguồn gốc,
Trường hợp các doanh nghiệp, tổ chức chưa có kinh nghiệm, chưa đủ điều kiện nhập khẩu vaccine theo quy định đề nghị liên hệ với các đơn vị đủ điều kiện nhập khẩu vaccine để phối hợp thực hiện. Đối với các đơn vị không có khả năng tiêm chủng, Bộ Y tế sẽ chỉ đạo các đơn vị trong ngành y tế tổ chức tiêm chủng vaccine cho người dân.
Đối với các địa phương, đơn vị có khả năng nhập khẩu, tiếp cận nguồn cung vaccine phòng Covid-19 nêu trên, Bộ Y tế sẽ tạo điều kiện cấp phép nhập khẩu, kiểm định.
Châu Anh








.jpg)
![[VIDEO] Thủy điện chạy đua tích nước trước nguy cơ El Nino 2026 [VIDEO] Thủy điện chạy đua tích nước trước nguy cơ El Nino 2026](https://mtcs.1cdn.vn/thumbs/540x360/2026/05/05/tn.jpg)


![[VIDEO] TP.HCM quán triệt quan điểm ‘không đánh đổi môi trường lấy tăng trưởng kinh tế’ [VIDEO] TP.HCM quán triệt quan điểm ‘không đánh đổi môi trường lấy tăng trưởng kinh tế’](https://mtcs.1cdn.vn/thumbs/540x360/2026/04/29/tn-3(1).jpg)









.jpg)





